FDA(抗痛风药非布司他显著增加死亡风险)
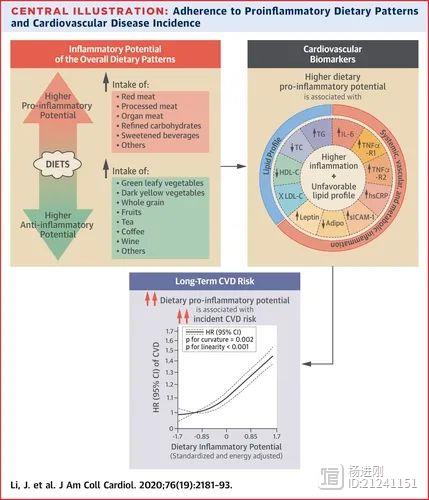
该研究纳入6000多例用非布司他或别嘌呤醇治疗的痛风患者,主要终点为首次心血管死亡、非致死性心肌梗死、非致死性脑卒中或需要紧急血运重建的不稳定性心绞痛;次要终点除了上述主要不良心脑血管时间,还包括全因死亡。
2月21日,美国食品药品监督管理局(FDA)发布消息称,痛风治疗药物非布司他(febuxostat)与临床常用的另一种降尿酸药物别嘌呤醇相比,显著增加心血管死亡和全因死亡风险,因此要求在该药的说明书上添加黑框警告。
2017年11月15日,FDA曾发布安全性警示公告称,一项安全性临床试验的初步结果表明,与别嘌醇相比,非布司他可能增加心脏相关性死亡的风险。
FDA此次得出的结论是基于一项大规模的上市后安全性研究。
分析结果显示,非布司他组的心血管死亡和全因死亡风险较别嘌呤醇组分别增加34%和22%。
早在2016年4月,加拿大卫生部就开展了一项安全性回顾分析,认为使用非布司他可能会增加心力衰竭发生或病情加重风险。
来源:FDA官网、国家药品监督管理局官网
FDA指出,非布司他仅可用于别嘌呤醇治疗失败或不能耐受别嘌呤醇的痛风患者。患者在应用非布索坦时应咨询其心血管风险,如在用药过程中出现胸痛、气短、心率增快或心律不齐、一侧肢体麻木或无力、眩晕、说话不利索、突发严重头痛等症状,应立即就医。
非布司他于2009年获FDA批准上市,2013年进入中国市场。
0000
评论列表
共(0)条相关推荐
我国台湾学者研究称,中风半年内停用他汀有危险
中国和欧美的相关指南均指出,他汀是脑中风后预防再次中风的关键药物,建议长期服用。但2010年调查显示,我国患者应用他汀的中风患者不足两成。近期,发表在《美国心脏协会杂志》的一项中国台湾研究表明,首次缺血性中风发作后3~6个月内如果停用他汀,1年内中风复发的风险显著增加。与缺血性卒中发作后一直坚持服用他汀的患者相比,3~6个月内停用他汀的患者卒中复发的风险增加42%,全因死亡风险增加37%。房颤合并多种疾病,死亡风险高!阜外医院杨艳敏等研究
阜外医院杨艳敏等研究发现,多发病和多药治疗在房颤患者中很常见,房颤患者多合并多种疾病和多种用药,而≥2种共病严重影响了患者预后。研究中,合并多种疾病和应用多药治疗的比例分别有67%和28.3%。研究发现,在评价随访1年期间,与≤1个共病的患者相比,≥2种共病患者的1年全因死亡增加1倍、心血管死亡增加1.5倍,大出血风险增加3倍。非阻塞性冠心病危险不容忽视!欧洲心脏杂志子刊研究
欧洲心脏杂志心血管影像子刊发表的CONFIRM注册研究提示,对于非阻塞性冠心病的患者,病变程度越重,危险因素越多,预后越差。非梗阻性冠心病是指患者出现心绞痛或病理上存在明确的冠脉粥样硬化病变,而冠脉造影未提示明显狭窄(<50%),甚至根本没有狭窄,冠脉CT可诊断非梗阻性冠心病。而如果没有冠心病,仅有糖尿病、高血压等传统危险因素并不增加全因死亡和非致死性心梗风险。AHA关于活性氧/活性氮与心血管病的科学声明十大必知要点
近日,AHA发布了关于活性氧与心血管病的科学声明,旨在为特殊的实验研究提供基本的思路。声明中指出,目前,尚无结论性证据表明活性氧/活性氮与心血管病有关,精确检测体内的活性氧/活性氮对后续的研究的开展至关重要。以下内容为本科学声明的科学要点:1自然界几乎所有真核细胞都能产生内源性的活性氧和活性氮,并且能自主调控体内这些活性物质的分化、迁移和代谢。细粮、红肉和甜饮料可让身体发炎!哈佛大学20万人研究
 杨进刚阜外2023-09-10 16:37:040000
杨进刚阜外2023-09-10 16:37:040000