3岁确诊肺动脉高压(母亲又怀孕3个月,能生吗,阜外医院遗传门诊案例)
为此逐渐停用了氨氯地平,改用双联肺动脉高压靶向药物治疗(安立生坦加量至 5 mg,每日1次联合他达拉非 5 mg,每日1次 )。
来源:吴艳,潘慧,叶梦婷,等. 儿童肺动脉高压的遗传检测与咨询一例. 中国循环杂志, 2022,37: 1156-1158.DOI: 10.3969/j.issn. 1000-3614.2022.11.013.【扫描二维码获取全文】
此案例中患儿母亲到遗传门诊看病时已经妊娠3个月,此时给患儿和家庭成员做遗传检测时间紧、风险大。
患儿全外显子组测序平均深度102.43X,20X覆盖度 98.7%。经参考序列比对,获得变异(SNV,indel)共计122 017个。在过滤掉人群频率超过 0.05或美国医学遗传学与基因组学学会(ACMG)指南明确为良性变异后,剩余1 446个变异,在此基础上又进一步筛查了22个肺动脉高压致病基因的罕见变异,在TBX4 基因上发现一个致病特征较强烈、达到ACMG评级疑似致病等级的杂合变异 c.109delC。
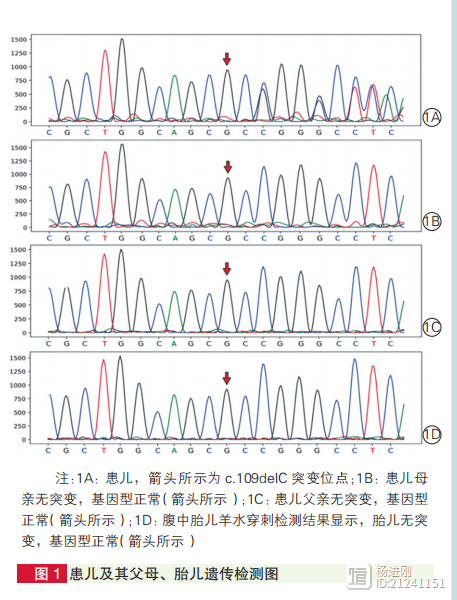
为进一步明确腹中胎儿基因型,与患儿母亲所在城市的妇产医院联系,经羊水穿刺术获得胎儿细胞,进行Sanger测序。如图1D所示,胎儿在目标变异 c.109delC 处不存在变异,为正常野生型,发生肺动脉高压的风险极低(百万分之五左右)。
此外,儿童遗传性肺动脉高压中有10%~20%为新生突变, 须高度重视儿童和父母核心家系的联合检测,以真正明确突变的来源及基因型-表型的共分离关系。
肺动脉高压具有很强的遗传特性,60%~80%的家族性肺动脉高压、20%~40% 的特发性肺动脉高压、10%~20%先心病相关性肺动脉高压均由基因突变引起。若未能及时发现突变基因的存在,突变将以50%的概率在家族中遗传,导致后代发病,给家庭和社会带来沉重负担。
当患儿明确携带TBX4基因突变后,临床分型从“特发性”肺动脉高压转变为“遗传性”肺动脉高压。
肺血管病与血栓遗传门诊制定了遗传检测方案:(1)先通过全外显子测序寻找患儿的致病基因;(2)通过一代测序明确父母基因型;(3)通过羊水穿刺明确腹中胎儿基因型;(4)结合临床给出遗传咨询建议。
患儿的TBX4 突变为新生突变,非父母遗传,腹中胎儿亦不携带,彻底打消了患儿母亲对腹中胎儿连续发病的担忧。

此病例中患儿右心导管中进行急性肺血管扩张试验提示开始为阳性,后逐渐转变为阴性,临床表型与基因型一致。
结果显示,患儿父母在TBX4 基因目标位置均为野生型(图1B、1C),进一步明确TBX4 基因型与肺动脉高压表型的共分离 [ACMG 中等致病证据(PM6)]。
这是一个极其罕见变异,在1 000 genome 数据库、ExAC数据库、EVS 数据库均无记载[ACMG 中等致病证据(PM2)]。
该变异位于TBX4基因的2号外显子,呈杂合形态,性质为移码突变,导致蛋白从第37位氨基酸截断(图 1A、图2),进而导致蛋白功能丧失 [ACMG极强的致病证据(PVS1)]。
患儿在其他肺动脉高压相关的基因上未发现可定级为疑似致病和致病等级的变异。
该患儿具有肺动脉高压早发(3岁发病)、特发(无其他诱因)、难治(5岁复发)等特点,提示可能存在潜在的遗传基因问题,但患儿4岁时曾接受遗传检测,并未找到明确致病基因。
为此,建议肺动脉高压患儿父母应尽早带患儿看遗传门诊,明确患儿基因突变后可利用试管婴儿技术阻断遗传性肺动脉高压在家庭的传递路径,确保下一个后代身体健康。
由于父母外周血基因检测正常,患儿携带的TBX4截断突变很可能(95%~99%)是新生突变,有极小可能性(1%~5%)是父亲或母亲生殖细胞的嵌合突变。
中国医学科学院阜外医院肺血管病与血栓遗传门诊接诊了1例5岁肺动脉高压患儿,同时其母亲已再次妊娠3个月。

由于携带此基因突变患者预后差,遂嘱咐其家长,患儿必须坚持长期用药,不能因病情稍有好转而停药,同时要长期密切随访,定期复诊,控制病情发展。
在明确患儿携带疑似致病变异TBX4 c.109delC后,对患儿父母的外周血 DNA 进行了Sanger 测序验证。
综上,TBX4 c.109delC具备ACMG指南中PVS1、PM2、PM6 三项致病性证据,且TBX4基因突变直接导致肺动脉高压,判定该变异为致病变异。
赵水平解读ADA糖尿病指南:几乎所有糖尿病患者需加用他汀
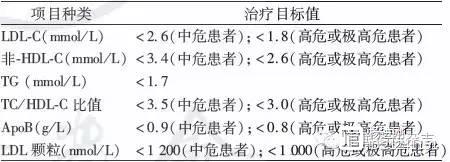
糖尿病患者多合并有血脂紊乱,如何更好管理糖尿病患者血脂?近期中南大学湘雅二院赵水平、赵旺等就此对近年来美国糖尿病学会(ADA)和美国内分泌医师协会(AACE)/美国内分泌学会(ACE)对糖尿病患者降脂的态度和推荐进行了对比和分析。几乎所有糖尿病患者在生活方式干预基础上应加用他汀 杨进刚阜外2023-08-02 11:50:300000
杨进刚阜外2023-08-02 11:50:300000Circulation文章称微血管病变在心肌缺血起关键作用:分为4型,用4条标准可诊断
近期,Circulation杂志刊登了了“缺血性心脏病再评价:冠状动脉微血管功能障碍在心绞痛病因中的基础作用”一文。文章指出,缺血性心脏病可由多种机制引起,包括心外膜冠状动脉狭窄、冠状动脉痉挛和冠状动脉微血管功能障碍(CMD)。作者说,“显而易见,冠状动脉微血管功能障碍在心肌缺血中起着关键作用。” 杨进刚阜外2023-08-23 12:44:410000
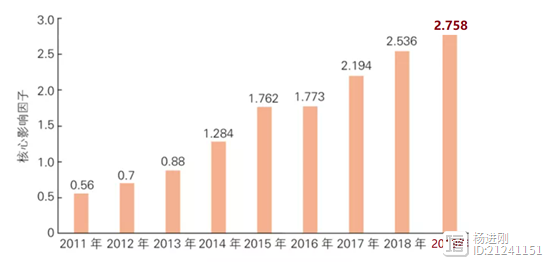
杨进刚阜外2023-08-23 12:44:410000蝉联心血管期刊榜首!中国循环杂志最新核心影响因子2.758
梅花报新春,牛年喜来到。中国科学技术信息研究所《2020年版中国科技期刊引证报告(核心版)自然科学卷》发布的结果显示,《中国循环杂志》核心影响因子再创新高,达到2.758,在21种心血管病学类期刊中再次排名第一。表12019年心血管病学类期刊核心影响因子前十名期刊名称核心影响因子数值核心影响因子排名中国循环杂志2.7581中华心血管病杂志2.0502中国心血管杂志 杨进刚阜外2023-09-13 16:57:230000
杨进刚阜外2023-09-13 16:57:230000中国循环杂志2015年十大事件
匆匆又是一年,《中国循环杂志》的全体员工团结一心,圆满完成了一年的工作,小有成绩。编辑部也评出了杂志社一年的十大工作成绩,也算是工作汇报吧。1、心血管中文期刊排名出炉,《中国循环杂志》位居第二;2、高润霖院士担任《中国循环杂志》总编辑;3、《中国循环杂志》刊载中国心血管病报告2014;4、《中国循环杂志》社出版2015年指南增刊;5、《中国循环杂志》社社举办临床戒烟研讨会;中年高血压、糖尿病和吸烟会让人“变傻”!
神经学杂志发表的一项研究提示,中年人群的心血管病危险因素,特别是高血压、糖尿病和吸烟或可能加快中年认知功能下降。研究发现,与非高血压患者相比,高血压患者的认知功能下降加快的风险增加了65%。吸烟者比不吸烟的人,认知功能下降加快的风险增加了87%。糖尿病患者比非糖尿病患者,认知功能下降加快风险增加1.5倍。而且危险因素数量越多,认知功能下降加快风险也越高。

 正在请求数据,请稍候!
正在请求数据,请稍候!