舒张性心衰试验为何鲜有成功(JACC文章另辟蹊径)
另外,专注于衰老生物学机制以改善与增龄相关的慢性病的老年医学手段,也可能有助于促进对舒张性心衰的理解和治疗。
1. 更好理解运动耐量下降的病理生理;

文章认为,舒张性心衰的治疗可能需要点特别的方法,而不是应用于年轻心血管病患者中的药物。
其他合并症扮演的角色
现在对于舒张性心衰,治疗手段也有限。不过近日2021年欧洲心脏病学会年会上公布的EMPEROR-Preserved研究传来好消息:对于舒张性心衰,不论是否合并糖尿病,常规治疗基础上使用恩格列净有助于降低患者心血管死亡或心力衰竭住院风险。
文章指出,鉴于虚弱对患病率和预后的影响,在考虑老年舒张性心衰患者治疗方案时,应以减轻症状、改善功能状态和运动能力为目的,以最终改善临床转归。
舒张性心衰与心外合并症相关,并部分受其驱动。
文章认为,将舒张性心衰定义为一种多系统老年综合征意义深远,或有助于解释为什么迄今为止药物干预试验碰壁。
这些因素会导致引起多器官功能障碍、虚弱以及心脏与骨骼肌疾病的毛细血管功能丧失、肌肉减少症、线粒体功能障碍和内皮细胞功能障碍。
此外最重要的是,这一定义还有助于将纯粹的以心脏为中心的管理方法,放大到综合的、患者整体意义的管理策略,将治疗重点转移到考虑患者自我报告的结果,包括生活质量状况、症状负荷以及运动耐受性、机体机能与认知状况等。
3. 明确可预防和缓解舒张性心衰患者运动耐力下降的新的、有潜力的目标;
而且舒张性心衰这一概念的改头换面,还指引了验证新药疗效的机会,比如那些有抗炎作用的、改善毛细血管活力的以及改善线粒体功能的药物。
值得注意的是,舒张性心衰的病生理学和临床表现存在明显的性别差异,其中女性患舒张性心衰的风险更高,终生风险是收缩性心衰的2倍。有研究显示,多于80%的老年女性心衰是舒张性心衰。
舒张性心衰:多系统老年综合征
入选我国113家医院3.5万例心衰患者的研究发现,中国心衰患者中,舒张性心衰占38.0%,收缩性心衰占40%。
以最大摄氧量(VO2peak)衡量的运动能力差,是老年人群舒张性心衰发展的独立预测因素。
另外,传统的单一器官为重点的管理手段可能对于总体老龄化、多种合并症和生理储备下降背景下的舒张性心衰是不适宜的。
虚弱是一种反映生理储备功能下降和对压力源脆弱的生物综合征,代表了与衰老异质性背后的关键因素
对于舒张性心衰患者运动耐力下降的机制,既往鲜有人关注,而这次会议则别开生面深入对心外相关因素进行了讨论,并提出“新的、综合的、循证的”路径,呈现了展开系列研究的机会。
来源:
其中参会者包括老年医学专家、老年病学专家、心脏病专家、运动生理学专家、骨骼肌生物学专家以及研究代谢与脂肪细胞的专家。
舒张性心衰最初被认为仅是由于左室舒张异常和左室顺应性降低所致,不过随着对其病生理的理解,多器官老年综合征逐渐浮出水面。
骨骼肌(肌肉减少症、氧气利用、内皮功能障碍)、肺和右心系统(肺功能和右心)、代谢紊乱(肥胖、糖尿病与胰岛素抵抗)、衰老机制(衰老、蛋白质稳态、炎症、衰弱)、生活方式干预(热量限制、运动、多方面体能干预)。
虚弱可通过增加合并症、慢性炎症、肌肉减少症负担以及功能储备整体下降导致患者严重的运动耐力下降。
此外有研究显示,新颖的康复干预有助于改善合并虚弱的舒张性心衰。
老年舒张性心衰患者直立运动期间,最大摄氧量较低。这意味着,对于健康成人微不足道的日常活动,这些患者却需要花最大的努力。
文章还指明了未来对老年舒张性心衰的研究优先侧重于以下四点:
这些变化不仅会导致心肌细胞的变化,还会导致脂肪、骨骼肌、自主调节、血液学、内皮细胞以及其他更为广泛的影响。
近日,欧洲心脏病学会发表的新版心衰管理指南很注重运动康复,鼓励慢性心衰患者参与力所能及的锻炼。
这提示,改善合并症是治疗老年舒张性心衰的重要策略。
而这篇文章就是美国国家老龄化研究所组织的一次工作会议头脑风暴的产物。
宏观上看,舒张性心衰患者运动耐力下降,不仅在于心脏特异性变化,而且在于更为广泛的衰老相关因素。
与年龄和性别匹配的健康人相比,舒张性心衰者的最大摄氧量平均降低 35% 。
有研究从亚细胞层面描述了增龄增加了暴露于心血管病脆弱性,而这也可能影响了舒张性心衰的发展,包括沉默调节蛋白、自噬和细胞衰老的变化。
舒张性心衰的发展与功能衰退与更低的呼吸困难与疲劳阈值有关。
舒张性心衰最初为老年科医生Robert Luchi所描述,而老龄化是舒张性心衰最强风险因素之一。当前患病率的增加,人口老龄化的推动出了不少力。

文章指出,运动耐力下降是一个理解舒张性心衰病理生理机制和最佳治疗的关键的、患者为中心的指标,而且独立于临床事件。
之前在健康成人中的研究显示,最大摄氧量随增龄而下降,而且在老年时下降更为显著,20岁到30岁每十年下降3%~6%,到70岁后每十年下降>20%。
一个人健康变老时,最大摄氧量也逐渐降低,但在无病情况下并不会引起运动耐力下降,即在正常日常活动中出现呼吸急促和疲劳。
近期,衰老的分子特点和亚细胞生物学的变化,已被认为是导致慢性增龄相关疾病的年龄相关变化的基本决定因素。
不论如何,发表在JACC上的一篇文章认为,应该重新思考对舒张性心衰的认识了。
舒张性心衰可能由炎症,或循环中源于肥胖尤其是腹部脂肪的其他因素所启动,特别是在多发病、衰老和缺乏体力活动情况下,腹部脂肪组织过多时。
舒张性心衰患者中有高75%的人伴有衰弱,老年舒张性心衰患者伴有衰弱预后更是雪上加霜。
近年来认为,舒张性心衰或是一种全身性、多器官疾病,而且与其他常见的、难以治疗的、衰老相关的疾病有某种共性。
合并症对老年舒张性心衰患者的影响甚收缩性心衰患者,而且这些较高负担的合并症可进步减低最大摄氧量,增加运动耐力下降。
4. 设计和验证跨学科干预措施以预防和减轻运动耐量下降。
而衰老与循环因素在促进舒张性心衰方面也得到一些异时共生研究的支持,比如将老年鼠和幼鼠通过外科手段连接起来后共用血液循环后,幼鼠中的生长分化因子-11 就有助于逆转老年鼠的舒张性心衰特征。
舒张性心衰也同其他老年综合征一样,合并症、虚弱和功能低下是舒张性心衰的临床核心表现.
2.基于病理生理基础,开发新颖的对不同舒张性心衰表型的分类方法;
文章认为,这提示,结合衰老与心血管病相关学科知识和概念或许能打开新窗口。
目前认识短板和未来研究方向
[1]AmbarishPandey, et al. Exercise Intolerance in Older Adults With Heart Failure WithPreserved Ejection Fraction: JACC State-of-the-Art Review. J Am Coll Cardiol.2021 Sep, 78 (11) 1166–1187.
此外,随着年龄增长,力量和平衡能力也会下降,这也加剧了因骨骼肌萎缩、力弱和线粒体呼吸受损等所致的最大摄氧量的缩减。
这些也与运动、减重之类的生活方式干预改善心脏和心外合并症的多效性一致,通过改善全身炎症、肥胖以及骨骼肌氧利用等改善舒张性心衰患者运动能力和生活质量。
文章还大篇幅阐述了心外因素所致舒张性心衰运动耐力下降的病生理机制,其中重要的认识差距有以下几方面:
运动耐力下降:舒张性心衰的关键表现

舒张性心衰“钟爱”老年人,提示了特定的年龄相关的之于舒张性心衰的脆弱性。
这些心外合并症约减少最大摄氧量的50%,通过运动训练可改善患者85%的最大摄氧量,此外,还对骨骼肌有所影响,而骨骼肌不同于心肌有再生和修复功能。
但是对于射血分数保留的心衰(舒张性心衰),也就是舒张性心衰,运动耐力下降(Exercise Intolerance)是主要的临床表现,而这种运动耐力下降的结果就是生活质量差。

BBC:乌龟不能随便养,出现这三种情况可能是细菌感染
美国疾控中心在8月31号称,数十名美国人从宠物乌龟身上感染了沙门氏菌。自三月以来,有37个人在接触乌龟后生病。其中十二个病人小于5岁,有些人已经住院,疾控中心称该疾病可能持续流行。感染沙门氏菌的症状包括腹泻、发烧和肚子疼。13个州都发现了该病,纽约州的患病人数最多。据今日美国报道,这不是美国第一次发生沙门氏菌。2015年和2013年就发生过,当时最为严重,感染病例接近500个。Europace杂志刊发阜外医院姚焰等新研究:继发于肺动脉瓣狭窄的室速很特殊
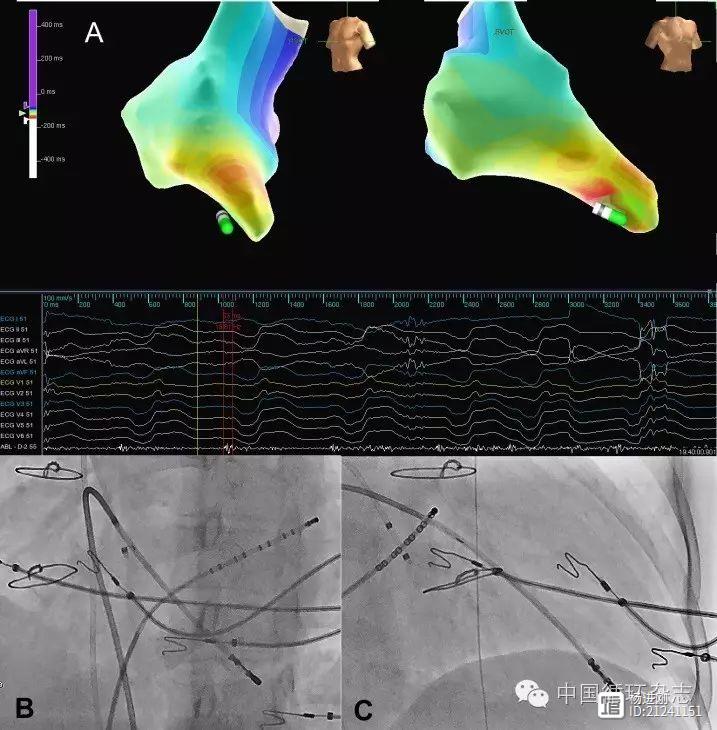
阜外医院姚焰团队新近在Europace杂志报告,继发于肺动脉(瓣)狭窄的室速机制具有特殊性,局灶性室速占了相当的比例,并且其局灶性激动最常见的部位似乎大多位于右室心尖部,与其他常见的右室局灶性室速部位明显不同。研究观察了5例接受了外科手术的肺动脉瓣狭窄患者,均分别于术后第4年至第10年发作持续性室速。 杨进刚阜外2023-08-04 08:55:170000
杨进刚阜外2023-08-04 08:55:170000房颤低卒中风险,要抗凝吗?欧洲心脏杂志研究
近期,欧洲心脏杂志的一项在瑞典、丹麦、挪威和苏格兰进行的一项多国近6万例房颤低卒中风险患者的研究表明,对于低卒中风险的房颤患者,与不治疗或华法林疗相比,服用新型口服抗凝药物治疗具有净临床益处。低卒中风险患者指CHA2Ds2-VASc评分男性为1分,女性为2分。研究发现,如果不治疗,缺血性卒中和出血的发生率均为为0.70/100人年。失眠 睡眠呼吸暂停最危险!澳大利亚研究
睡不着,睡着了又憋气,在很多人中可见。而一项来自澳大利亚弗林德斯大学的研究发现,有失眠和阻塞性睡眠呼吸暂停高风险的人死亡风险增加。这项研究共纳入7000多人,其中74%无失眠或阻塞性睡眠呼吸暂停,3%的人失眠,20%的人有阻塞性睡眠呼吸暂停,3.3%的人既有失眠也存在阻塞性睡眠呼吸暂停。 杨进刚阜外2023-09-30 08:40:390000
杨进刚阜外2023-09-30 08:40:390000每周吃3~<6个鸡蛋,可改善血脂!阜外医院China-PAR研究新分析
6月16日,阜外医院顾东风院士团队发表的China-PAR研究新分析结果提示,对于中国成年人来说,每周吃3~<6个鸡蛋,可明显改善血脂代谢。同时,研究者发现,吃鸡蛋较多(每周≥6个)对血脂,尤其是总胆固醇、低密度脂蛋白胆固醇、非高密度脂蛋白胆固醇,有明显的不良影响。实际上,2020年该研究团队发表的研究结果已经发现,每周吃3~6个鸡蛋时,全因死亡和心血管病风险最低。

 正在请求数据,请稍候!
正在请求数据,请稍候!