侧开胸(不停跳实施肝静脉,奇静脉连接术,阜外医院闫军团队巧治复杂先心病)
研究者指出,该术式可清晰显露肝静脉及奇静脉,避免再次正中开胸手术、应用体外循环及术中心脏停跳,避免过多心房切口引起心律失常等并发症。 同时,相比传统外管道全腔静脉- 肺动脉吻合术,肝静脉- 奇静脉连接术外管道短,血流耗能低,且可以使肝内血流平均分布于双肺,避免单侧肺因缺乏肝因子导致肺动静脉瘘。 他们表示,对于Kawashima 术后出现肺动静脉瘘的患儿,何时行肝静脉- 奇静脉连接术尚无定论。当怀疑或检查证实患儿存在肺动静脉瘘,血氧饱和度低于85% 且出现进行性活动耐量下降时,才建议行HAS。 术后该患儿吸入30% 的氧,血氧饱和度100%,血压、心律平稳,上、下腔静脉测压均为11 mmHg。机械通气6 h,重症监护病房住院2 d,胸腔引流管留置3 d,术后住院时间11 d;血氧饱和度处于98%~100% 之间。 术后10 d 复查心脏CT 及MRI示:下腔静脉肝段以远管腔通畅,未见明显狭窄或扩张改变,肝静脉- 外管道- 奇静脉吻合通畅,肝静脉血流平均分布双肺,上腔静脉- 肺动脉吻合口通畅。 由于置入外管道,患儿术后早期持续应用肝素抗凝治疗,后过渡用华法林抗凝,国际标准化比值控制在1.5~2.0后单用华法林。 他们表示,考虑静脉系统外管道问题,对于不存在高凝因素(快速性心律失常、既往血栓形成、蛋白S/ 蛋白C 系统及凝血功能异常等)的患儿,建议术后1 年口服抗凝治疗,此后可改用阿司匹林终生抗血小板治疗。 来源:董硕,段亚冰,王菊,等. Kawashima 术后行肝静脉-奇静脉连接术一例. 中国循环杂志, 2020, 35: 408-410.
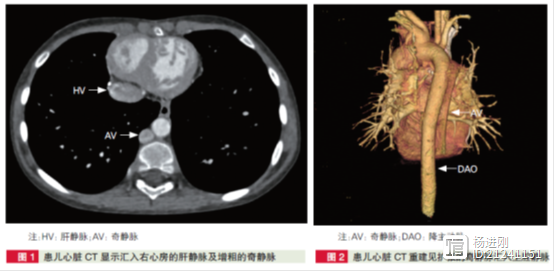
近期,阜外医院闫军团队报告了他们成功完成的一例Kawashima术后行肝静脉-奇静脉连接术。 在总结经验时,该团队指出,对于合并下腔静脉肝段缺如的患儿,建议Kawashima术后密切随访,为了避免肺动静脉瘘广泛形成,适时行肝静脉- 奇静脉连接术。 患儿女性,6 岁,4 年前曾在阜外医院行Kawashima手术,术后一般情况良好,血氧饱和度90%。 此次因活动耐量稍有下降、活动后口唇青紫,以“矫正型大动脉转位,肺动脉闭锁,室间隔缺损,房间隔缺损,下腔静脉肝段缺如,下腔静脉-奇静脉引流,主动脉右弓右降”入院。 入院血氧饱和度为80%,术前CT(图1、2)可见肝静脉及奇静脉均位于脊柱右侧,两根同等大小的肝静脉于膈肌上水平,共同汇入右心房,右心房汇入部、奇静脉横截面大小分别约22 mm×13 mm 和12 mm×13 mm。

血管造影可见主肺动脉及左、右肺动脉发育良好,上腔静脉- 右肺动脉吻合口通畅,奇静脉扩张明显,下腔静脉经奇静脉汇入上腔静脉,未见明显肺动静脉瘘形成,肺动脉收缩压/ 舒张压为19/13 mmHg。 闫军团队通过全面仔细评估,决定通过侧开胸、在非体外循环下为该患儿施行肝静脉-奇静脉连接术。 手术时,经充分游离肝静脉及右心房肝静脉汇入部、同一水平位置偏上方游离奇静脉后,常温下直接阻断奇静脉近心端及远心端,取14 号Gore-tex 管道与奇静脉行端侧吻合,随后开放奇静脉;于右心房肝静脉汇入部横断肝静脉,行肝静脉Gore-tex 管道端端吻合,缝闭右心房切口,两次阻断均未超过15 min,完成肝静脉- 奇静脉连接术(图3)。
最新Meta分析:GLT-2抑制剂改善心血管预后最好,DPP-4抑制剂无证据
近年来,二肽基肽酶-4(DPP-4)抑制剂、胰高血糖素样肽-1(GLP-1)受体激动剂、钠-葡萄糖协同转运蛋白-2(SGLT-2)抑制剂等新型降糖药物对心血管预后的影响成为医学界的热门研究点。血压超130/80有危险,改善生活方式可抵消!宁光等近10万中国居民研究
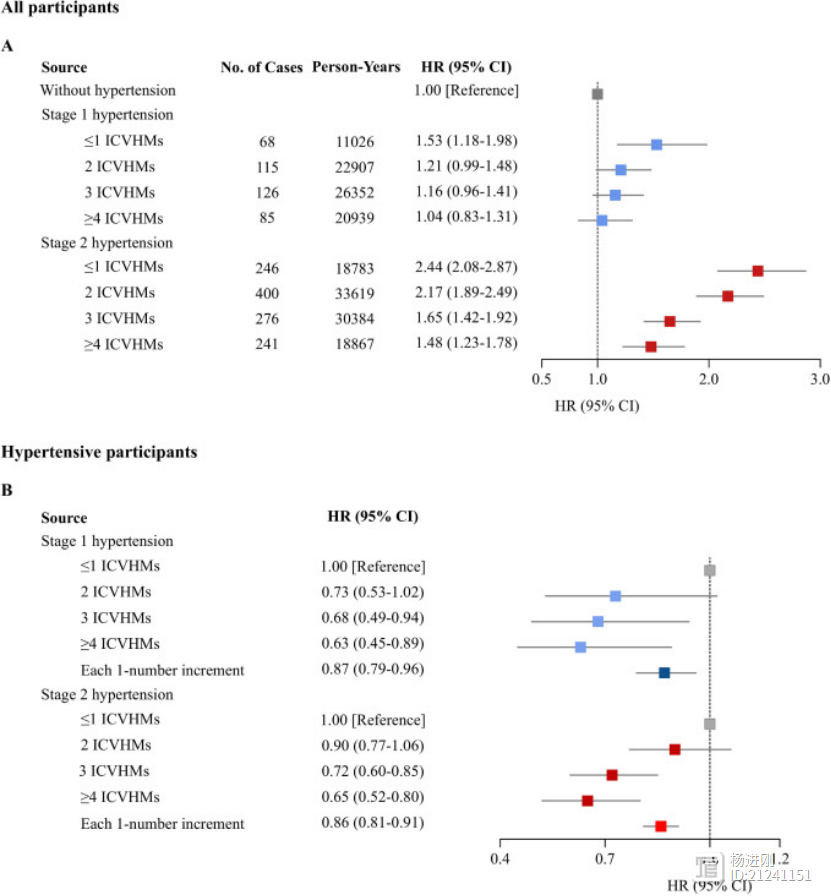
2017年发布的美国高血压指南建议,血压≥130/80mmHg即诊断为高血压,130-139/80-89为1级高血压。而目前我国高血压指南仍以血压≥140/90来诊断高血压,130-139/80-89属于高血压前期。此前已有不少国内外研究表明,当血压水平达到美国新指南定义的1级高血压时,心血管风险即已明显增加。 杨进刚阜外2023-09-22 15:55:590000
杨进刚阜外2023-09-22 15:55:590000医院职工最缺运动!我国四类社区近5万人生活方式分析
阜外医院胡安易、李希等对我国四类社区(医院功能社区、企业功能社区、城市居民社区和农村居民社区)46,846名35~60岁中年人数据进行分析后发现,在四种健康生活方式中,医院职工在不吸烟和少饮酒方面表现最好,但在充足身体活动方面却处于最低水平。四种健康生活方式包括不吸烟、不饮酒或适量饮酒、充足的身体活动和健康饮食。