癌症患者发生房颤怎么办?美国心脏协会肿瘤心脏学心律失常声明
近日,美国心脏协会(AHA)发表了心脏-肿瘤学心律失常和自主神经紊乱的识别、预防和管理的科学声明。
癌症和房颤有共同的危险因素
声明指出,癌症患者常有心律失常,而房颤最常见,也有心室复极异常和QT间期延长、室性心律失常、心动过缓和心脏传导阻滞等。
癌症患者发生心律失常可归因于抗癌药物的细胞效应、电解质异常或与癌症治疗相关的毒性,如心力衰竭、心肌缺血或心肌炎。
流行病学研究表明,癌症患者中房颤发生率较高,房颤患者中癌症发生率也较高,可能是因为有共同的危险因素。
癌症患者发生房颤与多种因素有关,包括高龄、代谢紊乱、电解质异常或炎症等。癌症的治疗也可能直接或间接导致了心律失常的发生。
但目前对高危癌症人群的房颤防治仍缺乏循证医学依据。
蒽环类药物可致左心室功能不全和心力衰竭,且呈剂量依赖性。在一项阿霉素研究中,有10.3%的患者发生房颤。
在蒽环类药物相关左室功能障碍患者,包括房颤在内的心律失常发生率达56.6%。
抗代谢药物、烷基化剂、铂类药物、小分子酪氨酸激酶抑制剂、免疫调节药物、免疫检查点抑制剂、嵌合抗原受体T细胞治疗、组蛋白脱乙酰酶抑制剂、抗微管类药物,这些抗癌药物都或多或少可致心律失常。
应用胺碘酮和地高辛要谨慎
针对癌症患者的房颤等心律失常的处理,与一般人群相似。其中房颤的治疗包括心率和心律控制,但特别要注意避免药物相互作用。
对于无症状的房颤患者,心率控制策略是合适的,管理目标是静息心率<110次/min。首选β受体阻滞剂。应谨慎使用非二氢吡啶钙拮抗剂(地尔硫卓和维拉帕米),因为其抑制CYP3A4代谢。
癌症患者应谨慎使用地高辛,因为许多抗癌药物都会抑制P-糖蛋白,升高地高辛浓度。
心动过速在癌症患者中常见。心动过缓也是多种治疗的副作用。
对于有症状房颤的患者,或因房颤心力衰竭恶化的患者,可考虑恢复和维持窦性心律。
抗心律失常药物尚未在癌症人群中进行研究,鉴于药物相互作用,因此必须谨慎使用这类药物。
因影响CYP3A4和P-糖蛋白系统,癌症患者应避免应用决奈达隆。
胺碘酮常被用于治疗癌症相关心律失常,但可增加各种癌症药物的浓度。
导管消融术在癌症治疗相关心律失常的治疗过程中是否有效尚未确定。
达比加群和利伐沙班抗凝需谨慎
对于活动性恶性肿瘤患者,动脉和静脉血栓很常见,合并房颤血栓风险更高,可考虑抗凝治疗。建议使用CHA2DS2-VASc评分决定是否抗凝。
建议CHA2DS2-VASc评分≥2分(男性)或≥3分(女性),且无明显禁忌证的患者抗凝治疗。
低分子肝素在预防深静脉血栓形成方面优于华法林,是癌症患者首选的抗凝药物,但没有研究评估其在房颤/扑动时的抗凝作用。
由于潜在的药物相互作用,抗癌药物可影响抗凝药物的选择。新型口服抗凝剂与P-糖蛋白系统相互作用,达比加群受影响最大。
利伐沙班和阿哌沙班也由CYP3A4代谢,因此,使用时必须谨慎将其与包括伊布替尼在内的诱导剂联合应用。
不推荐癌症患者应用阿司匹林用于预防房颤的相关血栓栓塞,因为癌症患者常伴随血小板减少和血小板功能障碍,面临出血风险高。
癌症患者抗凝治疗很复杂,包括药物相互作用和出血风险,左心耳封堵或许相对更安全有效,但到目前为止无相关研究。
监测QT间期
癌症患者QT间期延长的发生率高达22%。尽管对QT监测没有标准化的建议,有必要依据不同的药物定期心电图监测。
对于一种不知是否会导致QT延长的新药,建议在第一次给药后和每一次调整剂量后进行心电图监测。最终应制定肿瘤治疗的标准化QT监测方案。
一般来说,当QTc>500 ms或较基线变化>60 ms时,心律失常风险增加。如果发现明显的QT间期延长,应停止服用影响心脏复极的非必须药物,纠正电解质(尤其是钾和镁)异常。
出现室性早搏、室性心动过速或室性心动过速时,应立即采取纠正措施,包括输注硫酸镁,应用异丙肾上腺素或临时起搏将心率维持在>100次/min。美西律可能有助于减少砷引起的QT间期延长和复发性室性心动过速。
化疗引起的室性心律失常,包括持续性室性心动过速和心室颤动比较少见。
在接受化疗的晚期转移性癌症患者中,室性心律失常的发生率较高,但也可归因于癌症本身。
预防癌症患者心室颤动的重点是纠正危险因素,包括电解质紊乱,避免使用抗心律失常药物。
植入式心律转复除颤器(ICD)在化疗诱导的心肌病中的作用尚未得到明确的研究。
目前的指南建议,在左室射血分数≤35%的心肌病患者中使用ICD进行一级预防,并规范用药。
化疗引起的心肌病也可能伴有心脏传导系统异常,表现为宽QRS间期(>120 ms)。
目前支持癌症患者应用CRT都是基于病例报道。前瞻性MADIT-CHIC研究证实了化疗诱导的心肌病患者(左室射血分数降低≤35%,宽QRS波群)能从CRT中获益。
可考虑减少减慢心率药物
由于监测和报告的差异,与化疗相关的房室传导疾病发生情况不确定。应用不同类别的化疗药物可出现良性窦性心动过缓,很少发生症状性心动过缓和高度房室阻滞。
紫杉醇相关的可逆性无症状窦性心动过缓发生率高达30%,沙利度胺可导致多达40%的患者出现窦性心动过缓,其中一些患者因头晕和晕厥需要植入起搏器。5-氟脲嘧啶也与症状性或无症状性心动过缓有关。靶向治疗和免疫治疗也能引起心动过缓。
对于心动过缓,虽然还没有明确的预防策略,但是应用房室结阻滞药可能会增加心动过缓效应,因此,在开始癌症治疗之前,应考虑预防性减少剂量。
癌症患者和癌症幸存者自主神经功能障碍或神经系统失调的患病率高于健康人。癌症治疗期间或治疗后的有氧运动训练也被证明能逆转自主神经功能障碍。
除了增加盐和液体的摄入量、抬腿/压迫和避免使用血管扩张药物外,直立性低血压的治疗方案包括米多君、氟氢可的松、醋酸氟氢可的松、溴吡斯的明和屈西多巴。
尽管缺乏相关数据,但在该人群中,使用伊伐布雷定治疗症状性窦性心动过速可能是一个选择。
来源:Recognition, Prevention, and Management of Arrhythmias and Autonomic Disorders in Cardio-Oncology: A Scientific Statement From the American Heart Association. Circulation. 2021 Jun 17. Epub ahead of print.
转载:请标明“中国循环杂志”很多疑难复杂病例,一个医生一生也只能见到一次
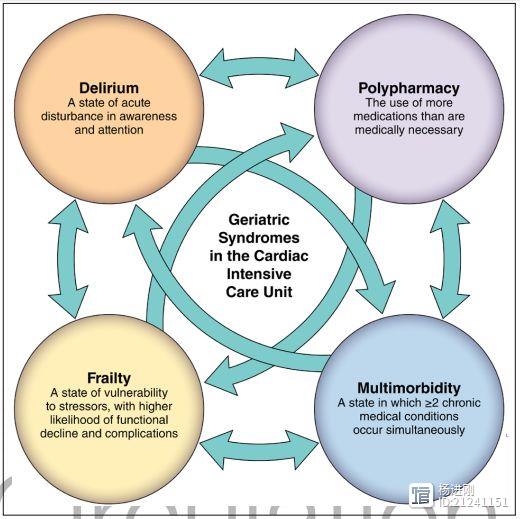
警惕衰弱、谵妄和认知功能下降!AHA发布心脏重症监护室老年人管理声明:鼓励适当身体活动,避免药物相互作用
12月9日,美国心脏协会(AHA)发布了心脏重症监护室老年人管理科学声明,提出要特别关注和处理好老年危重心脏病患者的老年综合征,包括包括衰弱、谵妄、认知功能下降、多种合并症、多重用药。 杨进刚阜外2023-08-31 09:51:220000
杨进刚阜外2023-08-31 09:51:220000美建议:医生应询问所有成年人是否吸烟
近日,美国预防医学工作组(USPSTF)成年人戒烟最终建议发布。新建议声明,医生应询问所有成年人是否吸烟,建议吸烟者戒烟,并向其提供有证据基础的行为治疗和药物治疗以协助戒烟。吸烟是减少疾病发病率、致残率及死亡的主要可预防因素。新建议是对2009年版的更新,于9月21日在线发表于《内科学年鉴》及USPSTF官网上。TIMI评分,可预测非阻塞性心梗预后!阜外医院俞梦越等研究
TIMI危险评分是目前常用的急性心梗患者危险分层评分体系。研究表明,TIMI危险评分对急性冠脉综合征患者主要不良心血管事件的发生具有较高的预测价值。近期,阜外医院俞梦越等发表的一项研究表明,TIMI危险评分同样可预测冠脉非阻塞性心梗患者的远期预后。 杨进刚阜外2023-10-01 22:06:490000
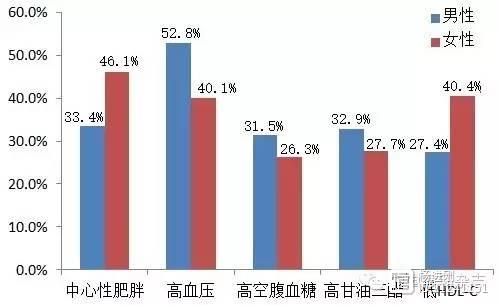
杨进刚阜外2023-10-01 22:06:490000最新研究提示:四分之一国人有代谢综合征
近期,吉林大学公共卫生学院一项纳入20余万人的荟萃分析结果表明,国人代谢综合征已成灾,患病率已高达24.5%。代谢综合征是一组以胰岛素抵抗为中心,聚集中心性肥胖、高血压、血脂异常、空腹血糖升高等多种心血管病危害因素于一体的病理状态。得了代谢综合征的患者罹患心脑血管病的风险是无此病者的3倍,病死率更是增加5~6倍。 杨进刚阜外2023-07-31 12:45:190000
杨进刚阜外2023-07-31 12:45:190000肝纤维化指标,还能预测心衰预后!河北学者Meta分析
河北省人民医院学者发表的一项Meta分析表明,一种原用于评估肝纤维化的简单指标——肝纤维化-4指数,还可预测心衰患者的预后。注:FIB-4:肝纤维化-4指数;AST:谷草转氨酶;PLT:血小板计数;ALT:谷丙转氨酶肝纤维化-4指数计算公式 杨进刚阜外2023-10-01 21:51:130000
杨进刚阜外2023-10-01 21:51:130000