免疫应答率100(陈薇院士团队柳叶刀报告全球首个新冠疫苗I期临床试验结果)
该研究显示,健康成年志愿者在接种以腺病毒Ad5为载体的新冠疫苗后,自接种第14天开始体内出现明显的抗体增长,并在接种第28天达到峰值;特异性T细胞反应在接种后第14天时达到峰值。 志愿者接种疫苗后28天内未发生严重不良反应。低、中、高剂量组接种疫苗7天内至少出现1种不良反应的患者比例分别为83%、83%、75%。 最常见的接种部位不良反应是疼痛,整个接种人群中有54%报告这个现象。最常见的全身不良反应是发热(46%),其次是乏力(44%)、头痛(39%)、肌肉疼痛(17%)。大多数不良反应是轻度或中度。 研究人员指出,该研究是目前报道的首个以腺病毒Ad5为载体的新冠疫苗1期临床试验,初步显示该疫苗的耐受性良好,能够诱导快速的免疫应答。该研究团队会继续对这些接种新冠疫苗的志愿者至少进行6个月的随访,届时将对疫苗的安全性和有效性进行进一步评估。 据澎湃新闻报道,根据《柳叶刀》杂志提供的资料,负责这项研究的陈薇院士表示,这项1期临床试验是一个重要的里程碑,表明新型5型腺病毒载体新冠疫苗有潜力被进一步研究。但应谨慎解释这些试验结果,因为开发新冠疫苗所面临的挑战是前所未有的,并且触发这些免疫反应的能力并不一定表明该疫苗将保护人类免受新冠病毒感染。 该研究于湖北武汉从2020年3月16日至3月27日筛选了195名健康成年志愿者,最终纳入108人,其平均年龄为36.3岁,男女基本各占一半,低、中、高剂量接种组各有36例。 据悉,陈薇团队已于4月12日启动新冠疫苗的Ⅱ期临床试验,纳入508名志愿者。 来源:[1]Safety, tolerability, and immunogenicity of a recombinant adenovirus type-5 vectored COVID-19 vaccine: a dose-escalation, open-label, non-randomised, first-in-human trial. Lancet, May 22, 2020[2] 柳叶刀发布陈薇团队新冠疫苗试验结果. 澎湃新闻
5月22日,军事医学研究所陈薇院士等在《柳叶刀》杂志在线发表了全球首个新冠疫苗I期临床试验结果:108名健康成年志愿者接种疫苗后28天全部产生了明显的细胞免疫反应。
转载:请标明“中国循环杂志”

中国50万人慢病研究给“为孩子操碎心”提供新注解:越多生育孩子,越易患心血管病
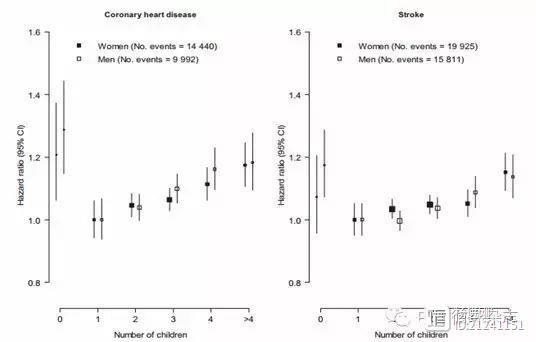
自古以来,中国家长就十分重视孩子的抚养和教育。尤其是现在的父母,不光要照顾孩子的饮食起居,还常常陪同孩子上辅导班,为孩子的学习成绩和前途而奔波、焦虑。有句话说的好,“为孩子操碎了心”。中国慢性病前瞻性研究近期发表的一项分析则显示,生育的孩子数越多,父母的冠心病和卒中风险越高,为这句话提供了新的“证据”。 杨进刚阜外2023-08-03 13:35:480000
杨进刚阜外2023-08-03 13:35:480000EuroPCR重新定义慢性冠状动脉综合征:生理影像学指导的介入治疗走上前台
大家都知道急性冠状动脉综合征,而在近期召开的EuroPCR2018上,慢性冠状动脉综合征(CCS)成了热门话题。心绞痛是慢性冠状动脉综合征的一个重要症状。此外,慢性冠状动脉综合征还影响生活质量(QoL),降低耐力,有精神症状、急症冠脉综合征复发住院等。德国诺伊斯医学院Lukas医院MichaelHaude在会上发布了发布了“稳定性冠心病经皮冠状动脉介入(PCI)治疗决策的PCR声明”。入院血糖高,冠脉介入后住院死亡风险增3倍!阜外医院袁晋青等研究
阜外医院袁晋青、许连军等研究发现,入院高血糖预示接受冠脉介入治疗的患者预后差。研究发现,与正常血糖组相比,高血糖组的住院期间全因死亡率和心原性死亡率均较高,高血糖组主要心脑血管事件发生率高于正常血糖组。Logistic多因素回归分析显示,高血糖使住院期间全因死亡风险增加3倍,心原性死亡风险增加4倍。